一例犬重症胰腺炎的诊治
摘要:
犬重症胰腺炎是宠物临床上较为常见的胰腺疾病,其发病急、病情危重、病死率高,临床上主要表现为厌食、呕吐、腹痛、腹泻、虚弱、脱水等。重症胰腺炎由于并发症多,诊断复杂,治疗往往不能解决疾病发生发展的主要矛盾,是宠物临床治疗上的难题。笔者在临床上接诊多例犬胰腺炎,现将一例犬重症胰腺炎的诊断与治疗过程介绍如下。
一、病史
6岁贵宾公犬,未去势,有胰腺炎病史,无手术史和药物过敏史。于2017年5月14号突然发病,表现为精神差,无食欲,小便少,没有又吐拉稀。发病前两天有大量进食肉类食品。15日去其他院诊治,经查体温39.4℃,血液生化检查显示肝肾功能指标未见异常,胰淀粉酶和胰脂肪酶指标高于生理正常范围,诊断为胰腺炎复发,针对胰腺治疗3天后未见好转且呕吐加重,小便减少。再次检查结果确定胰腺炎并发肾衰。18~24日对胰腺炎和肾衰抗感染和输液对症治疗,但治疗结果仍不理想,犬精神极差,厌食、呕吐、衰弱、小便少而黄。遂于26日转至本院。
二.临床检查
经检查患犬神情呆滞,不能正常站立,严重消瘦(体重由12的日3.14kg减至26的日2.45kg),重度脱水。全身皮肤通红,毛发无光泽凌乱,胸部皮肤破溃化脓,两前肢关节肿胀化脓感染(如图1)。全身浅表淋巴结无明显肿大。舌前端大面积发黑、坏死,口腔黏膜轻度黄染。眼球凹陷,分泌物较多,结膜潮红并黄染。体温(T):37.2℃,呼吸(P):18次/分,毛细血管再充盈时间(CRT):约3s,血压(BP):86/71mmHg。心率157次/分,律齐,未闻及病理性杂音。肺部听诊无明显异常。腹部干瘪,触诊未发现明显的异常包块,腹壁紧张。
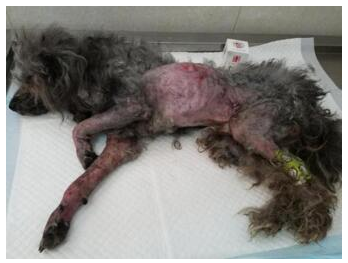
图1.就诊时的体况
三.实验室检查
1. 血常规检查
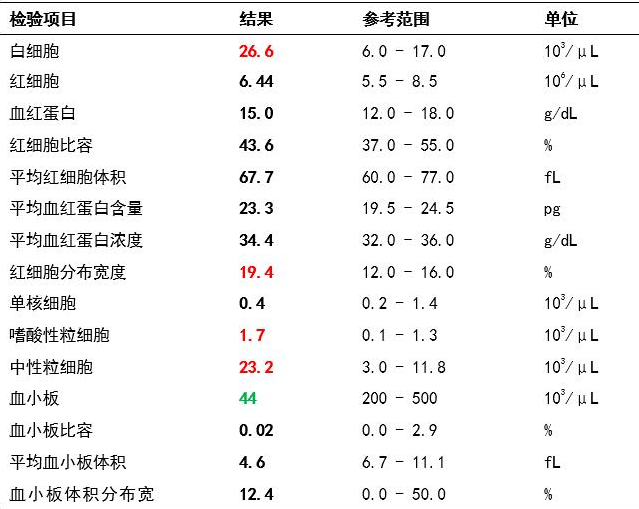
血常规检查结果见表1,可见病犬白细胞、嗜酸性粒细胞和中性粒细胞数量明显增多,血小板数量明显减少。提示机体可能存在感染,且血液凝集功能紊乱。
表1 血常规检查结果
2. 血液生化与血气检查
血液生化结果见表2,该犬α-胰淀粉酶远高于生理值,尿素氮、肌酐、总胆红素、肌酸激酶、碱性磷酸酶、血磷、γ-谷氨酰转移酶和天门冬氨酸氨基转移酶均高于生理范围。血钙、血钾和白蛋白均明显低于生理范围。提示可能胰腺、肾脏、肝胆管异常和机体离子代谢紊乱。
表2 血液生化与血气检查结果
3. 检测板检查
初步排除犬瘟病毒、细小病毒、冠状病毒和传染性肝炎病毒感染的可能,具体结果见表3。SNAP@cPL呈阳性,提示胰腺炎。
表3 快速检测板检查结果

4. 病理学检查
粪便镜检未发现明显虫卵。
腕关节处浓汁镜检可见大量中性粒细胞和球菌(如图2)。
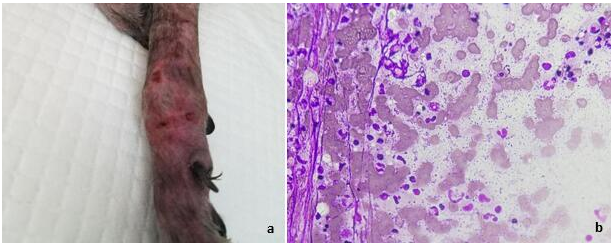
图2.腕关节:a.关节旁脓肿;b.浓汁涂片镜检
四.影像学检查
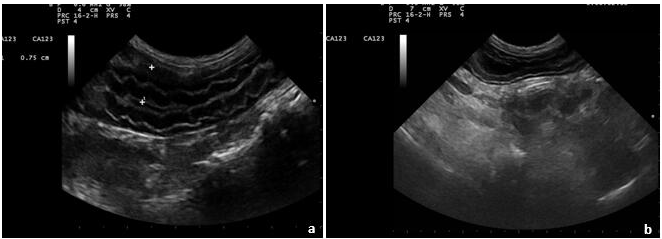
B超检查:肝脏大小形态未见异常,肝内未发现强回声病灶,胆管回声增强,未见明显结石。十二指肠肠壁呈现不规则样皱缩,明显水肿增厚,达到7.5mm(如图3.a)。胰腺明显肿大,以胰头和胰体部更为明显,胰腺内可见多个强回声区域,胰腺与周围脂肪分界不清,胰管呈现强回声(如图3.b)。双肾未见明显肿大,形态结构未见明显异常。X光检查:未见明显异常。

图3. 腹腔B超检查:a.十二指肠水肿增厚; b.胰腺明显肿大和回声增强及胰管强回声
五.诊断
综合病史、临床检查和实验室检查诊断为:重症胰腺炎并发急性肾损伤、胆管炎、炎症性肠病和深层脓皮症。其诊断依据如下:
A.胰腺炎:
1.该犬有胰腺炎病史,且发病前两天有大量进食肉类餐桌食品,这可能是引发胰腺疾病的原因;
2.临床上主要表现为精神极差、厌食、呕吐、衰弱、严重脱水,腹部触诊敏感,全身皮肤通红等;
3.发病初期从当地医院检查结果显示胰淀粉酶和胰脂肪酶指标高,肝肾等生化指标均在生理范围,提示可能存在胰腺炎;
4.本院检查结果显示胰淀粉酶远高于生理值,SNAP@cPL呈强阳性,WBC和CRP均高于生理正常范围等,B超显示胰腺明显肿大,且胰腺上有多个强回声区域,可确诊为胰腺炎。
B.并发急性肾损伤:
发病初期生化结果显示BUN和CRE均在生理范围,但由于脱水的发展,在发病后第4天血清BUN升高,而CRE未升高且处于生理范围,在发病后第13天BUN和CRE均升高。可见胰腺炎为原发病,肾功能损伤为继发性。
C.并发胆管炎:
血液生化结果中GGT和ALP的明显升高以及B超可见胆管的回声增强,提示胆管炎。胰腺炎发病过程中,会释放大量的胰酶到附近组织器官和血液中,导致附近器官的损伤。因此结合临床症状和本院就诊前肝脏生化各指标未见异常判断胆管炎为胰腺炎继发的可能性较大。
D.并发炎症性肠病:
B超结果显示十二指肠肠壁呈现不规则样皱缩,且明显水肿增厚(如图3);虽然该病例没有做组织活检,但结合临床消化道症状和典型的B超影像也可确诊为炎症性肠病。胰腺炎发病过程中由于各种炎性因子和激活状态下的胰酶刺激,可继发导致炎症性肠病。
E.并发深层脓皮症:
两前肢腕关节旁皮肤化脓破溃,胸部皮肤深层化脓感染,浓汁抹片镜检可发现大量中性粒细胞和球菌(如图2),可确诊为深层脓皮症。
F.休克与重症胰腺炎:
就诊时该犬神情呆滞,体温低,严重脱水,血压低且脉压差低于20mmHg,CRT大于2s,初步判断为休克。结合上述临床症状和检查结果可确诊重症胰腺炎。
六.治疗原则与方法
重症胰腺炎的治疗应积极补液扩容,纠正酸碱平衡和电解质紊乱,应用抗生素防止感染性休克,抑制胰酶活性和生成,疼痛管理,对症治疗等。由于该重症胰腺炎已出现多种并发症,且机体处于休克状态,因此整个治疗应分轻重缓急。
第一阶段:重点缓解机体的休克状态,同时控制胰腺炎对机体的进一步损伤和抗感染治疗;
第二阶段:重点防治胰腺炎对机体的损伤,同时进一步抗感染治疗和缓解肝肾损伤;
第三阶段:各并发症的治疗。
1.输液治疗。
对重症胰腺炎的治疗主要是输液治疗,根据监测的血气电解质和生化结果,选择合适的液体,及时纠正电解质酸碱平衡紊乱,维持水、电解质和酸碱平衡,血氧饱和度低时吸氧维持正常的血氧饱和度。维持机体正常血容量和血液循环系统的稳定,改善微循环,可有效缓解机体休克状态,同时也可缓解肾脏并发症和防止全身其它并发症的发生。
2.应用抗生素。
胰腺炎感染的细菌多源于肠道常驻菌群,革兰氏阴性菌和厌氧菌为主的混合感染。目前认为对于重症胰腺炎常采用对胰腺有较好渗透性的抗革兰氏阴性菌或广谱抗生素,同时联合应用对厌氧菌有效的甲硝唑。本病例中针对WBC明显增高和深层脓皮症,应用1mg的麻保沙星和10mg的甲硝唑联合应用,抗感染治疗。
3.抑制胰酶活性和胰腺分泌。
本病例采用乌司他丁联合奥曲肽使用来控制体内胰酶的活性和生成。胰酶抑制剂乌司他丁可有效抑制胰酶活性,同时调节凝血功能改善胰腺微循环障碍,也可抑制多种炎性因子的活性,在控制胰腺炎及其导致的全身性炎性反应中发挥重要的作用。奥曲肽可有效抑制胰酶的生成。两种药物的联合使用可以有效可抑制多种炎性因子,对控制胰腺炎及其导致的全身性炎性反应发挥重要的作用。
4.禁食和营养支持。
重症胰腺炎发病初期为了减轻胰腺分泌排泄,特别在呕吐时一般不能喂食。加上机体处于高营养代谢,需营养支持,一般采用全胃肠外营养。本病例中由于机体处氮质血症,为了减轻肝肾的负担,仅采静脉输注用葡萄糖和维生素维持机体的营养和能量需求。当呕吐得到有效控制后,少量多次的低脂肪低蛋白(婴儿米粉)的进食,同时给予静脉营养,促进胃肠蠕动和疾病恢复。
5.对症治疗。
呕吐:胃复安和维生素B6的使用;胆管炎:口服清肝利胆药(熊去氧胆酸);
深层脓皮症:皮肤体表炎性分泌物的清理和腕关节处脓肿的清洗,化腐生肌膏(百灵金芳)的使用,全身抗生素的使用;
炎症性肠病:消除可能病因(细菌感染,胰腺炎),肠道炎症的控制,促进肠道功能的恢复,采用艾灸疗法。
6.止疼。
由于本病例中患犬疼痛表现并不明显,存在肝肾损伤,因此不利于肾脏恢复的非甾体消炎药并未使用。然而阿片类的止疼药在国内宠物临床上的使用管控较严,也没有使用。
七.治疗结果
该犬入院后,诊断为重症胰腺炎并发急性肾损伤、胆管炎、炎症性肠病和深层脓皮症。经综合治疗后病情缓解,于治疗21天后出院。出院时能正常进食,大小便未见异常,血常规、生化和血气电解质各指标均恢复生理范围;彩超肠壁厚度和蠕动状态未见异常;两后肢根骨处皮肤破溃已完全愈合,其他部位皮肤均已恢复;口腔舌头坏部分已脱落且伤口已恢复。
疾病的治疗恢复过程如下:
A.经过第一阶段3天的抗休克治疗,病犬已脱离休克状态,精神明显好转,能缓慢行走,呕吐得到明显控制,自己排小便,体表皮肤和腕关节处感染已得到明显控制。肾脏主要指标BUN和CRE均恢复至生理范围,血气电解质相对稳定,但胰腺重要指标AMY仍高于2200IU/L,cPL也呈强阳性。
B.经过第二阶段8天重症胰腺炎的控制,病犬已脱离危险,精神基本无明显异常,腹部触诊未发现明显异常,没有呕吐和拉稀,食欲逐渐恢复,有自主采食行为,体表皮肤和腕关节处感染和破损已恢复,舌头坏死部分脱落,但根骨部皮肤仍有破溃。肝肾主要指标ALT、AST、BUN、CRE均在生理范围,血气和电解质监测结果未见异常,ALP和GGT也持续下降,ALP从815IU/L下降至547IU/L,GGT从14IU/L下降至9 IU/L。胰腺指标AMY从大于2200IU/L下降至1367 IU/L,cPL仍呈强阳性。
C.经过第三阶段10天的并发症调理,该犬已能自主进食且各指标均恢复正常,体重2.40kg。体表皮肤愈合良好。出院两周后复查各指标无异常,饮食正常,体重2.55kg。
八.讨论
犬胰腺炎指多种病因导致胰酶胰酶(胰蛋白酶原、胰凝乳蛋白酶原、弹性蛋白酶原、前磷脂酶A、前辅脂肪酶等)被激活后对自身及其他组织器官的消化,导致水肿、出血甚至坏死的炎症反应。该病的各个阶段所表现出的临床症状和检查结果各不相同,从轻度的食欲减退和精神沉郁到重度的剧烈呕吐、拉稀带血、休克甚至死亡[2]。重症胰腺炎是胰腺炎发病过程中引起多组织器官的损害,成为急性胰腺炎的多种并发症和致死原因[1]。本病例中患犬已经出现黄疸、脱水、皮肤大面积化脓溃疡、舌炎坏死和休克等危重症状,结合临床检查结果诊断为重症胰腺炎。
犬胰腺炎的发病机制尚未完全清楚,目前有局部血循环障碍、胆管疾病蔓延、肠道细菌异位继发感染、胰导管阻塞、肠胰返流和传染性疾病(CDV)等。虽然犬胰腺炎的发病病理机制有所不同,但都存在胰酶对胰腺自身的消化。正常情况下,胰腺腺泡细胞内酶的形成与分泌过程处于与浆细胞隔绝状态,胰腺分泌的各种酶进入十二指肠前均处于无活性或微活性的酶原状态;同时正常胰管具有黏膜屏障作用,它可以抵挡少量胰酶的消化作用;胰腺实质与胰管,胰管与十二指肠之间存在压力差,因此一般情况下,十二指肠液不会反流入胰腺。临床上暴饮暴食是急性胰腺炎发病的常见原因之一,除此之外药物和毒素、胰导管阻塞、十二指肠内容物反流或者其他疾病诱发都可能导致胰腺炎的发生[3]。患犬主诉发病前两天有大量进食肉类餐桌食品,在短时间内一次性大量摄入高蛋白及高脂肪类食物,可刺激胰腺快速分泌大量胰液,管腔内压力增大,同时过多的胰液不能快速通过胰管进入十二指肠,则可能倒流入胰腺组织,致使胰腺发生“自我消化”[3],因此推测大量进食肉类餐桌食品是该犬胰腺炎发病的主要诱因。
犬胰腺炎临床症状与常见的消化道疾病症状相似,其诊断需结合病史、症状、实验室检查及影像学检查作出诊断。实验室检查结果主要表现在白细胞的升高,CRP和cPL呈阳性反应,AMY升高。虽然血常规和血清生化指标检测可以反应机体的炎症病变,但是对胰腺炎的诊断都是非特异的。目前临床上使用的IDEXX公司的SNAP cPL胰腺炎快速检测板,虽然具有较高特异性,但临床上笔者还是会结合腹部彩超来诊断。如果B超显示胰腺在回声上发生变化(即低回声或回声增强提示胰腺坏死,胰腺周围高回声提示胰周脂肪坏死)具有高度的特异性[4]。在犬由于肾脏参与胰酶的清除,犬的重症胰腺炎由于血液循环中过量的胰酶对肾脏的消化损伤很容易并发出急性肾功能不全,肾功能不全时由于胰酶清除障碍也容易导致血浆胰酶的升高并导致胰腺炎,因此在临床诊断过程中,不容易区分肾功能不全并发胰腺炎的原发病因。患犬来本院就诊前AMY高和cPL呈阳性,同时肾脏的主要指标BUN和CRE结果未见异常,因此可以推测胰腺炎的发生在肾功能不全之前。最终的治疗结果也印证了胰腺炎继发肾功能不全的诊断结果。
犬重症胰腺炎病情危重,发展迅速,并发症多,死亡率高,且其导致多器官功能障碍的发病机制尚未完全阐明。随着宠物诊疗技术的发展,虽然犬胰腺炎的治疗有了进一步的突破和发展,但对于犬重症胰腺炎的治疗仍然是临床上棘手的问题。在人医临床研究发现重症胰腺炎死亡因素中急性肾衰竭、CT严重指数、多器官功能障碍综合征、休克、红细胞压积下降等均能增加重症胰腺炎的死亡率[5]。
对于重症胰腺炎的治疗,首先应该重视发病过程中可能危及动物生命的并发症,只有迅速缓解严重并发症,使患病动物脱离重症危像。患犬转诊至本院时机体已经处于休克状态,实验室检查结果显示重症胰腺并发急性肾损伤和严重深层脓皮症。因此,第一阶段我们治疗的侧重点是机体的抗休克、抗感染治疗,同时兼顾胰腺炎及各并发症的治疗:1.根据血气电解质监测结果针对性的输液扩容和电解质酸碱度的纠正,维持正常血压,保证机体各组织器官的正常血液灌注。2.静脉注射2000IU乌司他丁和严格禁食禁水。乌司他丁由于其具有广谱高效抑制酶活性的功能,同时能缓解胰酶入血介导炎性细胞对多器官的损伤,抑制多种炎性介质如TNF-α、I-6、I-8等从而抑制炎症的扩大发展,减少全身性炎性反应的发生;缓解疼痛与抑制外周P物质产生有关;抑制血小板活化因子(PAF),调节血管内皮功能,改善胰腺微循环及减轻组织损伤;抑制心肌抑制因子(MDF),阻断急性胰腺炎引起的休克[6]。严格的禁食禁水可以减少食物对胰腺的刺激。3.抗生素的使用:在转诊至本院前已连续十多天头孢类抗生素的使用,但机体仍然处于明显的感染状态,时间不允许笔者做药敏实验,于是根据临床经验笔者采用联合低剂量麻佛微素(1mg)和甲硝唑(10mg)的抗感染治疗。4.其它并发症的对症治疗。如止吐药胃复安的使用,对抗氧化自由基对胰腺的损伤和促进皮肤愈合药维生素C的使用等。值得注意的是:本阶段虽然存在急性肾损伤,但本阶段的治疗并未使用肾损伤过程中常用的利尿剂呋塞米,因为患犬有很好的输液反应,即输液后能自主排小便,同时呋塞米的使用可能会加重胰腺的损伤和不利于机体低血容量性休克的缓解;虽然皮质激素的使用可以帮助机体平稳度过休克状态,但患犬此时处于严重的感染状态,同时皮质激素的使用不利于胰腺炎的恢复[7]。经过3天的治疗,机体已经脱离休克状态,且肾脏功能得到明显恢复,疗效可观。
机体的休克缓解,患犬的治疗进入第二阶段,即重症胰腺炎的综合治疗。
1.尽量找出并排除诱发因素,并在治疗过程中避免这些因素的干扰。本患犬推测的可能原因是暴饮暴食。因此在治疗的呕吐阶段为了避免食物对胰腺的进一步刺激[8],综合考虑还是禁食禁水。有学者认为在理想状态下,治疗同时应当恢复饮食,绝食会导致肠粘膜厚度及小肠绒长度下降[9]。但是在实际临床上笔者一般会在治疗过程中直至24小时内未发生呕吐反应,且有食欲再尝试性缓慢喂食原味婴儿米粉或粥。
2.密切监测血气电解质,并根据结果常规补液、纠正酸碱电解质平衡。维持机体的营养需要和保证胰腺正常微循环灌注。
3.抑制胰腺分泌和胰酶的活性。采用SS类似物奥曲肽和胰酶活性抑制剂乌司他丁的联合使用。奥曲肽可抑制胃肠分泌尤其是胰腺的分泌;抑制平滑肌收缩;且可松弛Oddi括约肌降低胰管内压力,同时能清除有氧自由基,减少炎性因子释放,从而阻止胰腺炎的进一步发展[10]。
4.细菌感染的控制。犬重症胰腺炎时肠道细菌可移居其它组织器官继发感染,因此在补液的同时要应用抗生素进行抗感染治疗[3]。患犬第一阶段的抗感染效果较好,因此本阶段不考虑更换抗生素。此阶段的治疗持续了8天,患犬脱离危险能自主采食。
经过第二阶段的治疗患犬虽然已脱离危险,且肾脏指标恢复正常,彩超显示胰腺结构回声未见异常,但重症胰腺炎并发的炎症性肠病并未完全缓解(彩超显示肠壁厚度依然高于正常达到7mm,且肠道蠕动缓慢),单次进食量稍大就会出现呕吐。胰腺炎快速检测板cPL依然呈强阳性。体表皮肤及腕关节处化脓感染已得到控制,但后肢根骨处皮肤未愈合。
目前炎症性肠病的病因不清,可能与肠道淋巴组织缺陷、贫血、精神因素、生化紊乱、遗传和药物不良反应等有关[4]。在人医临床有研究显示胰腺炎发病过程中IFN-γ和TNF-α等炎症因子参与炎症性肠病的发生[11]。针对炎症性肠病的治疗主要治疗药物为:皮质类固醇、氨基水杨酸类药物和免疫调节剂。如同所有疾病一样,最佳的治疗无疑是针对病因治疗,患犬在治疗的前两个阶段机体处于重度感染状态,因此不建议采用上述治疗炎症性肠病的药物,而是针对机体的休克,感染和重症胰腺炎的控制。到了第三阶段虽然炎症性肠病的缓解较慢,但也可能与发病初期长时间的禁食有关,于是随后采用艾灸疗法治疗,隔姜片艾灸双侧足三里、脾俞和胃俞,每天每个穴位艾灸20分钟左右。艾灸温养脾胃、疏调肠腑气机的治疗方法对炎症性肠病效果显著。艾灸可刺激穴区局部温度感受器,提高穴区肥大细胞脱颗粒率,通过调控转录因子影响靶器官肠道免疫相关因子的表达,以及促受损肠粘膜屏障修复而发挥抗炎作用,同时有防治肠纤维化的作用[12]。经过一周艾灸治疗,彩超显示肠道的水肿增厚状态明显改善,肠道蠕动缓慢得到明显缓解。对cPL呈阳性的问题,由于彩超显示胰腺形态结果尚可,笔者此时并未做特殊处理,仅控制饮食,从饮食的角度去做调理,给予犬低脂易消化处方狗粮和婴儿米粉搭配少量红狗营养膏。调理10天后复查,指标均处于生理范围。患犬根骨部皮肤愈合缓慢可能与该犬治疗后期活动过程中与外界的摩擦有关。有研究结果证明奥曲肽对外科伤口愈合有显著的副作用,其损害作用程度与氢化可的松相当[13]。因此可推测根骨部皮肤愈合缓慢与重症胰腺炎治疗过程中奥曲肽的使用也会影响伤口的愈合。对此笔者对患犬根部伤口涂抹重组牛碱性成纤维细胞生长因子凝胶后覆盖适当大小的消毒辅料,适当包扎处理,效果显著,约一周后愈合。
犬重症胰腺炎的发病症状各不相同,并发症多,临床表现多种多样,其治疗需要结合症状、实验室检查和影像学检查结果,准确诊断的基础上,针对不同病因、症状和并发症制定不同的治疗方案。
重症胰腺炎治疗应该先急后缓,优先处理危及生命的并发症,如休克、低血压、呼吸系统综合征、急性肾损伤和多器官功能障碍等,同时加强监护和胰腺炎的兼顾治疗。胰腺炎的治疗原则首先解除或纠正发病因素;输液纠正血气电解质酸碱平衡,维持正常血容量,保证胰腺血液灌注,初期肠外营养的给予;胰酶分泌的抑制和胰酶活性抑制剂的使用;抗生素的合理选择;其他并发症的控制以及尽早的恢复饮食。
参考文献
[1] 庞勇斌,吕云福.影响重症胰腺炎预后的危险因素.中国热带医学.2009,9(3):492-493.
[2] Richard W.Nelson,C.Guillermo Couto. Small animal internal medicine. Third
Edition:535-543.
[3] 董路.犬胰腺炎的诊断和治疗.[硕士学位论文]. 陕西:西北农林科技大学,2016.
[4] Cynthia M.Kahn, Scott Line. 默克兽医手册. 第十版:264-265.
[5] 黄辉.我国重症急性胰腺炎死亡因素Meta分析.[硕士学位论文]. 遵义:遵义医学院.2014.
[6] 戴妮,丁明星.乌司他丁联合奥曲肽治疗犬急性胰腺炎的效果观察.中国畜牧兽医.
[7] Watson PJ, Rouloisa,Scaset, et al.Prevalenceandbreed distributionof chronic pancreatitis at post mortemin firstopinion dogs. J Small Anim Pract.2007.
48:609-618
[8] 张谊,徐泽涛,罗祖华,詹成波. 一例北京犬急性胰腺炎的诊治[J]. 湖北畜牧兽医,2012,(01):26-27.
[9] 谢华丽.某宠物医院犬胰腺炎临床病例分析及诊疗报告.[硕士学位论文].陕西:西北农林科技大学,2014.
[10] Hoogerwerf WA. Pharmacological management of pancreatitis. Curr Opin Pharmacol, 2005, 5(6): 578-582.
[11] 陈佩钦,徐红梅. Mucin 1的异常表达:炎症性肠病和胰腺炎的桥梁[J]. 中国肿瘤生物治疗杂志,2011,(01):16.
[12] 马喆,张慧,王茎,李垠和. 艾灸治疗炎症性肠病的古代文献与现代研究的思考及展望[J]. 世界科学技术-中医药现代化,2016,(12):2188-2193.
[13] 戎文慧. 奥曲肽对小鼠伤口愈合的副作用研究[J]. 北京军区医药,1997,(06):474-475.